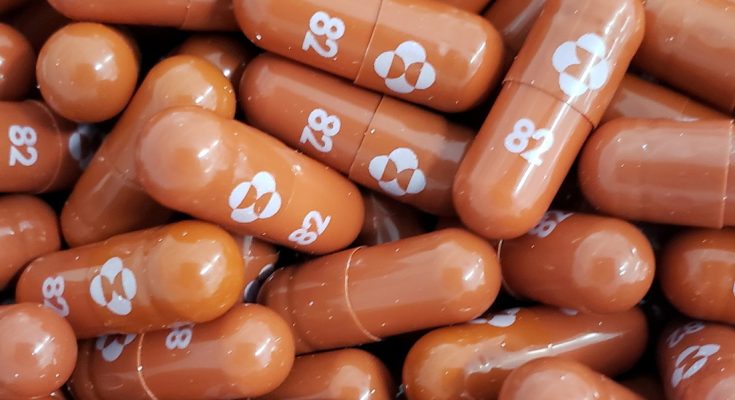
La pastilla experimental anticovid que desarrolla Merck en colaboración con la empresa de biotecnología Ridgeback Biotherapeutics, este fármaco redujo a la mitad el riesgo de hospitalización o de muerte en los pacientes con covid-19 que participaron en su ensayo clínico.
El medicamento, identificado como MK-4482/EIDD-2801 o molnupiravir, es un agente antiviral oral experimental contra el covid-19 descrito por Merck como un “potente análogo de ribonucleósido que inhibe la replicación del Sars-CoV-2, el agente causante del covid-19”. El fármaco, concebido inicialmente por la Universidad Emory y adquirido por Merck, consiste en una pastilla que se administra por vía oral dos veces al día durante 5 días.
De forma similar a otros medicamentos antivirales, el molnupiravir aprovecha la circunstancia de que el virus necesita multiplicarse en las células de una persona para contagiar, por lo que funciona gracias a bloques parecidos a ARN que introduce en el genoma del agente patógeno cuando se multiplica paralizando su replicación.
El fármaco de Merck sigue llamando la atención de la comunidad científica y de los medios de comunicación como alternativa a los tratamientos antivirales actuales contra el coronavirus que se administran por vía intravenosa. Frente a estos medicamentos, el molnupiravir parece lograr un beneficio competitivo, siendo más fácil y rápido de administrar, ya que la persona contagiada podría tomar la pastilla nada más percatarse de los síntomas de la enfermedad y recibir el diagnóstico sin atención médica adicional.
 Durante las fases preliminares de los ensayos con hurones, el medicamento de Merck mostró una eficacia consistente, neutralizando en 24 horas por completo la transmisión del virus SARS-CoV-2 y reduciendo significativamente la carga viral en el tracto respiratorio superior de los animales infectados.
Durante las fases preliminares de los ensayos con hurones, el medicamento de Merck mostró una eficacia consistente, neutralizando en 24 horas por completo la transmisión del virus SARS-CoV-2 y reduciendo significativamente la carga viral en el tracto respiratorio superior de los animales infectados.
En la III fase de los ensayos clínicos avanzados, se evaluaron los datos de 775 pacientes —algunos de los cuales recibieron molnupiravir y otros placebo— que presentaban un contagio de leve a moderado, con mayor probabilidad de mala evolución de la enfermedad debido a problemas de salud, como obesidad, diabetes o enfermedades cardiovasculares. Si bien estaba prevista la participación de cerca de 1.550 personas, la inscripción para el estudio fue detenida por los resultados positivos que ha demostrado.
Según explica Merck, el molnupiravir ha demostrado ser activo en varios modelos preclínicos del coronavirus, como la prevención, el tratamiento y la prevención de la transmisión. Asimismo, se ha descubierto que tienen una eficacia consistente frente a variantes comunes del covid-19 como Gamma, Delta y Mu.
Sin embargo, aún no se ha realizado un estudio exhaustivo sobre la posible mutagenicidad del molnupiravir, ya que las mujeres embarazadas quedaron excluidas del estudio, lo que hizo imposible la evaluación de su impacto en el feto. Asimismo, tanto los hombres como las mujeres que participaron en el estudio fueron obligados a abstenerse de mantener relaciones sexuales o de utilizar métodos anticonceptivos durante los ensayos clínicos.
Pese a los resultados positivos, el molnupiravir aún no ha recibido la autorización por parte de las autoridades sanitarias, por lo que se desconoce la fecha exacta del inicio de sus ventas.
Según el comunicado de Merck, el Gobierno de Estados Unidos ya compró 1,7 millones de dosis del medicamento por 1.200 millones de dólares. Asimismo, Merck, que planea fabricar 10 millones de pastillas antes de fin de año, ha firmado acuerdos de suministro y de compra de molnupiravir con otros gobiernos de todo el mundo, a la espera de la autorización reglamentaria.
Según se desprende de la suma pagada por el Gobierno estadounidense, el precio del medicamento podría llegar a los 700 dólares por cinco días de tratamiento.
F:https://actualidad.rt.com/actualidad/406712-farmaceutica-merck-avanzar-desarrollo-pastilla-molnupiravir